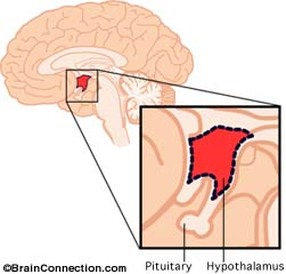
Undirstúka (Hypothalamus) og heiladingull (Hypophysis eða Pituitary Gland)
|
Undirstúku má greina í kjarna sem eru þó ekki mjög vel afmarkaðir berum augum og starfræn tengsl eru ekki að fullu rannsökuð. Sumir kjarnar framleiða fleiri en eitt hormón og sum hormón eru framleidd í fleiri en einum kjarna. Þeir tengjast innbyrðis og fá tengingar víða að.
|
Undirstúka er það svæði heilans sem situr ofan Chiasma Opticum og heiladinguls og milli þriðja heilahólfsins, Lamina terminalis og Corpora mammillaria. Undirstúka tengist heiladingli með stilki. Þó undirstúka vegi einungis u.þ.b. 4g (af um 1200g heilans) er hún aðalleikari hvað varðar samvægi (homeostasis) margra grundvallarferla:
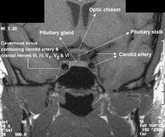
Stærð heiladingulsins er einnig í talsverðri mótsögn við starfrænt mikilvægi hans (0,6g og 6x13x9mm; hxbxd).
Heiladingullinn er staðsettur aftan við Sinus Sphenoidalis, í beinbolla er kallast tyrkjasöðull (Sella Turcica). Til beggja hliða er Sinus Cavernosus og í honum sitja heilataugar 3, 4, 6 og hlutar 1 & 2 af fimmtu tauginni. Auk þess situr þar A. Carotis en ofan við heiladingulinn er Chiasma Opticum (sjá mynd). Heiladingullinn er í nánum starfrænum tengslum við undirstúku og framleiðir fjölda hormóna. Heiladingullinn skiptist í fremri og aftari hluta sem eru af ólíkum fósturfræðilegum uppruna. Hvert um sig eru heiladingulshormónin einungis hluti af flóknum fram- og afturvirkum stýrikerfum sem hafa mjög víðtæk áhrif. Sem dæmi er ACTH sem er þannig hluti af því sem enn er kallað HPA-axis (hypothalamic - pituitary - adrenal axis) þó ljóst sé orðið að þetta nafn er einföldun því kerfið nær m.a. einnig til hippocampus og markvefjanna sjálfra þar sem nokkur afbrigði ensímsins 11beta-hydroxysteroid dehydrogenasa ráða miklu um endanleg áhrif kortisóls. Flóknir fram- og afturvirknisferlar eru þannig dæmigerðir. Ekki eru allir þessir ferlar vel þekktir ennþá og sífellt bætast við ný hormón og viðtakar sem virðast oft jafn mikilvæg og gömlu hormónin. |
- Aftari hluti heiladinguls er útvöxtur heilans sem inniheldur taugafrumuenda hvers kroppar tilheyra Supraoptic (SON) og Paraventricular (PVN) kjörnunum en þessir taugaendar losa AVP (ADH) og Oxytocin.
- Fremri heiladingullinn fær hinsvegar blóðborin boð frá ýmsum kjörnum sem losa sín boðefni í portal æðar heiladingulsstilksins: ACTH er losnar undir áhrifum CRH og AVP sem koma fofr frá PVN en einnig SON.
- GH losun örvast af GHRH frá Arcuate kjarnanum en er latt af somatostatíni sem fofr kemur frá PVN á periventricular svæðinu. Ghrelín kemur einnig við sögu.
- TSH er undir stjórn TRH sem kemur frá Dorsomedial kjarna.
- Prólaktín er eina hormónið undir tónískri bremsu dópamíns frá Arcuate kjarna.
- GnRH frá Arcuate og Preoptic kjörnunum stýrir LH og FSH losun en nýlega uppgötvaðist enn eitt hormón í undirstúku sem gegnir einnig hlutverki í losun GnRH en það kallast Kisspeptín og er aftur framleitt í Arcuate kjarnanum.
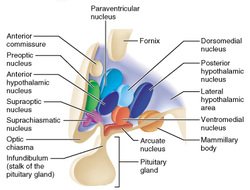
Suprachiasmatic kjarninn (SCN) er talinn gegna lykilhlutverki hvað varðar dægursveiflu hormóna og samhæfingu dagsbirtu, vöku og svefns. SCN er þannig sá gangráður sem virðist stjórna Paraventricular (PVN) (og SON) sem aftur stjórnar losun ACTH og síðan kortisóls.
Þessi hormón eru reyndar ekki bara losuð með circadian takti stýrt af SCN heldur einnig með ultradian takti en PVN virðist einnig hafa hlutverk sem gangráður með taktinn 1-3 losun/klst. PVN hefur einnig efferenta til autonom kerfisins sem aftur hefur áhrif á perifer (dæmi: lifur og aukin gluconeogenesis að morgni) og central (pineal gland: melatonin) líffæri.
Hitastjórn er mjög flókið fyrirbæri og virðist sem hugsanlegt sé að ekki komi endilega sömu svæði undirstúku að kælingu annarsvegar og hitamyndun hinsvegar. Helstu svæði sem skipta máli eru Preoptic og Posterior kjarnarnir en einnig Dorsomedial og PVN. Stjórn á matarlyst, orkubrennslu og líkamsþyngd hefur fengið mikla athygli á undanförnum árum. Við rannsóknir hafa uppgötvast ný hormón eins og Leptín, Ghrelín og Orexín en einnig hafa skýrst nokkuð tengsl og hlutverk ýmissa vel þekktra hormóna eins og insúlíns og GLP-1. Allmörg þeirra hormóna sem að þessu stjórnkerfi koma eru upprunnin perifert, t.d. í görnum og fituvef en undirstúka gegnir þarna lykilhlutverki og helstu kjarnar sem koma þar að eru Arcuate og PVN. Önnur hormón / boðefni sem mikilvæg eru í þessu sambandi eru: CART, POMC, NPY, PYY3-36, Agouti Related Peptide (AGRP) og Oxyntomodulin en listinn telur nú nokkra tugi hormóna.
Þessi hormón eru reyndar ekki bara losuð með circadian takti stýrt af SCN heldur einnig með ultradian takti en PVN virðist einnig hafa hlutverk sem gangráður með taktinn 1-3 losun/klst. PVN hefur einnig efferenta til autonom kerfisins sem aftur hefur áhrif á perifer (dæmi: lifur og aukin gluconeogenesis að morgni) og central (pineal gland: melatonin) líffæri.
Hitastjórn er mjög flókið fyrirbæri og virðist sem hugsanlegt sé að ekki komi endilega sömu svæði undirstúku að kælingu annarsvegar og hitamyndun hinsvegar. Helstu svæði sem skipta máli eru Preoptic og Posterior kjarnarnir en einnig Dorsomedial og PVN. Stjórn á matarlyst, orkubrennslu og líkamsþyngd hefur fengið mikla athygli á undanförnum árum. Við rannsóknir hafa uppgötvast ný hormón eins og Leptín, Ghrelín og Orexín en einnig hafa skýrst nokkuð tengsl og hlutverk ýmissa vel þekktra hormóna eins og insúlíns og GLP-1. Allmörg þeirra hormóna sem að þessu stjórnkerfi koma eru upprunnin perifert, t.d. í görnum og fituvef en undirstúka gegnir þarna lykilhlutverki og helstu kjarnar sem koma þar að eru Arcuate og PVN. Önnur hormón / boðefni sem mikilvæg eru í þessu sambandi eru: CART, POMC, NPY, PYY3-36, Agouti Related Peptide (AGRP) og Oxyntomodulin en listinn telur nú nokkra tugi hormóna.
Sjúkdómar í heiladingli
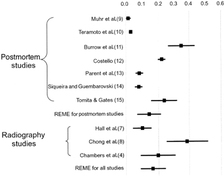
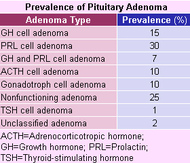
Ef frá er talin offita (sem færa má gild rök fyrir að sé tauga-innkirtlasjúkdómur), hafa klínískir sjúkdómar í heiladingli og undirstúku hinsvegar oftast verið taldir sjaldgæfir á öllum aldursskeiðum þó sumir séu með frægustu sjúkdómsmyndum læknisfræðinnar (spot diagnosis) eins og Cushing´s Disease og Acromegaly. Algengustu vandamálin sem upp koma í starfsemi undirstúku og heiladinguls stafa af æxlum sem verða til á svæðinu eða þá eru afleiðingar meðferðar við æxlunum. Algengustu æxlin í heiladingli eru prólaktín-framleiðandi og álíka algeng eru æxli sem ekki virðast framleiða neitt. Giskað hefur þó verið á að heildaralgengið sé um 17% sbr. þessa mynd hér f. ofan til hægri en hér að neðan til vinstri eru u.þ.b. innbyrðis hlutföll æxlistegunda tíunduð.
Æxli í heiladingli voru áður flokkuð eftir hefðbundnum vefjafræðilitunum (basofíl, krómófób o.s.frv.) en þessi flokkun á nú undir högg að sækja. Nú eru æxlin yfirleitt flokkuð eftir starfsemi (ákvarðað skv. hefðbundnum blóðmælingum og klíníkk) en enn nýrri er flokkun skv. ónæmisfræðilegum litunum (immunohistochemistry) vefjasýna. Að endingu má nefna mikilvæga einfalda klíníska flokkun sem byggir á mati segulóm-mynda en hún skiptir æxlum í microadenoma (<1 sm) og macroadenoma (>1 sm). Microadenoma valda sjaldan röskun á starfsemi heilbrigðs aðlægs hluta heiladingulsins.
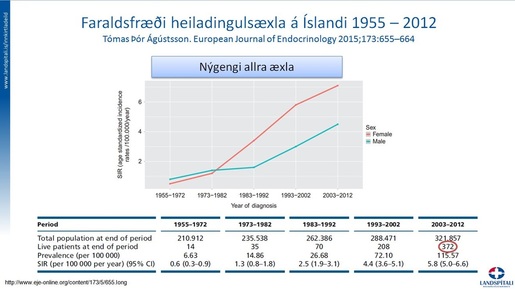
Faraldsfræði á ÍslandiSjúkdómsmynd æxla í heiladingli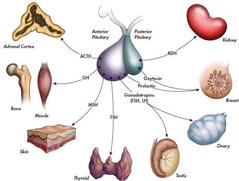
Ljóst má vera að raskanir á starfsemi undirstúku og/eða heiladinguls geta haft alvarlegar og fjölskrúðugar afleiðingar - þessi litlu líffæri taka til starfsemi nær allra annarra líffæra og stjórna grundvallarferlum eins og æxlun, svefni, næringu og líkamshita.
Klínísk mynd sjúkdóma í heiladingli ræðst fyrst af eðli grunnsjúkdómsins. Dæmi er Acromegaly sem stafar af æxli sem framleiðir vaxtarhormón. Fjölkerfa sjúkdómar eins og Sarcoidosis geta lagst á heiladingul og truflað eðlilega starfsemi á sértækan eða almennan hátt. Dæmi um sértæka truflun er t.d. Diabetes Insipidus einn og sér en dæmi um almenna röskun er Hypopituitarism. Fyrirferðir í heiladingli eru stöku sinnum meinvörp illkynja sjúkdóma annars staðar í líkamanum en eiga þó lang oftast ættir að rekja til heiladingulsfrumnanna sjálfra.
Staðbundin áhrif eins og höfuðverkur eru vegna togs á heilahimnur eða þrýstings. Adenoma í heiladingli vaxa oft ífarandi (þó þau séu annars góðkynja) og geta því valdið leka á mænuvökva. Mikilvæg líffæri í grenndinni eru Chiasma Opticum, Heilataugar 3, 4, (5) og 6 auk Art. Carotis Interna. Bitemporal hemianopia er klassísk afleiðing æxla í heiladingli. Craniopharyngioma eru sjaldgæf suprasellar/hypothalamic æxli sem helst greinast í börnum/unglingum. Þar sem þau geta truflað starfsemi undirstúku geta einkenni þeirra m.a. verið hyperphagia, poikilothermia, hydrocephalus og diabetes insipidus.
Verkferill vegna æxlis í heiladingli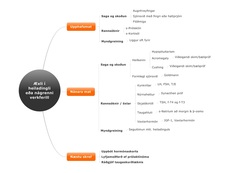
Eftir að hafa spurt í þaula um klínísk einkenni einstakra heilkenna og skoðað vandlega heilataugar, sjónsvið og önnur kerfi eftir atvikum (t.d. eistu hjá körlum grunuðum um hypogonadisma) eru tekin blóð eða þvagsýni til rannsókna. Mikilvægt er að biðja um bráðamælingu á prólaktíni ef viðkomandi hefur macroadenoma (þvermál >1sm) því ef það reynist prolaktínóma er skurðaðgerð yfirleitt ónauðsynleg. Hormón undirstúku og heiladinguls eru eins og áður hefur komið fram, dæmigert losuð í púlsum (mínútur - dægur osfrv). Ein blóðmæling dugar því sjaldnast til rannsókna. Hér er því rétt að minnast boðorða kirtlavina:
|
Ekki-starfandi æxli og hypopituitarism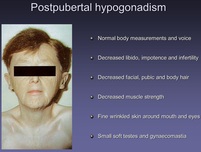
Algengustu æxlin (ásamt prólaktín framleiðandi æxlum) í heiladinglinum eru byggð frumum sem ekki virðast framleiða neitt (séu notuð hefðbundin blóðpróf) og eru því kölluð non-functioning eða núll-æxli. Þessi æxli eru nú reyndar flest talin vera svokölluð gonadotropinoma, þ.e. þau virðast framleiða LH, FSH eða alfa-undireiningar þessara hormóna en oftast er um að ræða óvirk afbrigði sem ekki mælast í hefðbundnum blóðprófum.
Þessi æxli valda einkennum f.o.fr. vegna stærðar og ífarandi vaxtar eins og áður hefur komið fram. Þannig getur raskast starfsemi einstakara annarra hormóna en oftast gerist þetta reyndar eftir ákveðinni röð (VH - LH/FSH - ACTH - TSH) og þegar öll eru biluð kallast ástandið panhypopituitarism en í fyrstu er um að ræða klíníska ástandið hypogonadism. Meðferð við þessum æxlum er fyrst og fremst skurðaðgerð (trans-sphenoidal). Margir hafa þó áfram skort á einstökum eða fleiri heiladingulshormónum og þurfa því eftirlit innkirtlalæknis til langframa. Algengt er að æxlin vaxi aftur og þá má grípa til geislameðferðar. PrólaktínæxliSkortur á prólaktíni veldur ekki - að því er best er vitað - einkennum. Hins vegar eru góðkynja prólaktínframleiðandi æxli ásamt núll-æxlunum algengustu æxlin í heiladingli. Ofgnótt prólaktíns er reyndar oftast af orsökum öðrum en æxlum.
Áhöld eru um það hvort microprolaktinoma (<1sm) séu í raun æxli sem þurfi meðhöndlunar við. Þannig eru margir sem telja að við minniháttar hyperprolaktinaemiu þurfi ekki endilega að gera segulómun og etv. ekki einu sinni að meðhöndla nema einkenni séu svæsin. Önnur heiladingulsæxli valda oft vægri hyperprolaktínaemíu vegna "disconnection". Einkenni karla með prólaktínóma eru oft alvarlegri en kvenna þar sem þeir kvarta seint:
Prólaktínóma svara mjög vel lyfjameðferð með dópamín agonistum og skurðaðgerðir eru nær alltaf óþarfar. Bromocriptine var fyrsta lyfið en nú eru komin nýrri lyf með vægari og öðruvísi aukaverkanaspegil: cabergoline og quinagolide.
Acromegaly (Æsavöxtur)Allir kannast við Jóhann Svarfdæling en eins og alkunna er hafði hann gigantismus sem er afleiðing adenoma í heiladingli sem framleiðir ofgnótt vaxtarhormóns. Myndist adenomað eftir kynþroska veldur það Acromegaly.
Vaxtarhormón hefur víðtæk áhrif á nánast öll líffæri mannslíkamans. Þessi áhrif eru hinsvegar mjög hægfara og Acromegaly greinist yfirleitt ekki fyrr en áratug(um) eftir upphaf sjúkdómsins (á fimmtugsaldri) og algengi er 60-70/1.000.000 íbúa. Nú má skima auðveldlega eftir þessu ástandi með mælingu á IGF-1. Til staðfestingar á greiningu þarf hins vegar að gera bælipróf sem í þessu tilfelli er 75g sykurþolspróf enda er seyting vaxtarhormóns eitt af varnarviðbrögðum líkamans við blóðsykurfalli. Um þriðjungur vaxtarhormónsframleiðandi æxla framleiðir einnig prólaktín. Meðferð við Acromegaly er fyrst og fremst transsphenoidal skurðaðgerð en á seinni árum hafa komið fram somatostatin hermar (t.d. octreotide) sem haldið geta framleiðslu vaxtarhormóns í skefjum og nota má fyrir og/eða eftir aðgerð. Skortur á vaxtarhormóni er aftur á móti ekki óalgengur fylgifiskur heiladingulsaðgerða og þarf á stundum að bæta upp. Sjúkdómur CushingsSjúkdómur þessi er eitt af dramatískari heilkennum læknisfræðinnar þó hann sé mjög sjaldgæfur. Sjá nánari umfjöllun hér.
Diabetes Insipidus (Þvaghlaupssýki)Polydipsia og polyuria (þorsti og þvaghlaup) einkennir þennan óalgenga sjúkdóm. Þvagið er hypotonískt miðað við plasma og magnið er oft mun meira en 5 lítrar á sólarhring. Cranial DI orsakast af skorti á ADH (eða Vasópressíni: AVP) og algengasta orsökin er aðgerðir og áverkar á heiladinguls-undirstúku svæðinu. Æxli eins og craniopharyngioma eða sjúkdómar eins og hypophysitis og sarcoidosis eru einnig orsakavaldar.
Vatnsskerðipróf er notað til greiningar en það greinir sömuleiðis milli cranial og nephrogenic þvaghlaupssýki (hypokalaemia, lithium, hypercalcaemia), en í því síðarnefnda er ekki skortur á ADH, heldur virkar það ekki á marklíffærið nýrun. 
AVP er mikilvægasta hormónið sem kemur að vatnsbúskap en það hefur einnig aðrar verkanir eftir því hvaða viðtaki virkjast í marklíffærinu. Helsti vaki AVP losunar er osmolality í plasma. Þetta er numið í osmoreceptor í hypothalamus. Einnig blóðrúmmál, metið í vinstri gátt og blóðþrýstingur, metinn í bulbus carotis og aortaboga. Að auki getur ógleði, hypoxia, hypoglycaemia, stress og hypercarbia haft áhrif. Þröskuldur losunar er oftast 280 mosm/kg (heldur lægra í þungun) en eðlileg gildi osmolalitets plasma er 285-295 mosm/kg. Eftir að AVP virkjar V2 viðtaka blóðrásarmegin í safngöngum nýrna eykst magn vatnsganga (Aquaporin-2) í frumuhimnunni við collecting duct lumenið. Collecting ducts verða þá gegndræp fyrir vatni og nýrun geta haldið því eftir og þvagrúmmál minnkar. Skortur á AVP eða bilun í nefndum viðtökum leiðir af sér sjúkdómsástandið Diabetes Insipidus (DI) sem er þá annað hvort cranial eða renal (nephrogenic).
Meðferð við cranial DI felst í gjöf DDAVP (inj., nefúði, töflur) sem er samtengt afbrigði af vasópressíni sem er sértækur V2 agonisti með lengri helmingunartíma og minni æðavirkni en hið náttúrulega vasópressín (sem er einungis 15 mín). |
Hyponatraemia og SIADH
Eðlilegt gildi natríums í sermi er um 135-145 mmol/l. Allt að 30% þeirra sem leggjast inná sjúkrahús á hverjum tíma hafa s-Na+ < 135mmol/l sem er oftast merki um hypo-osmolality enda er Na+ mikilvægasta osmovirka sameindin samanber eftirfarandi formúlu í SI einingum sem nota má til að reikna út serum osmolality.
s-osmolality = 2x[Na] + glúkósa + úrea
Einkenni hyponatraemiu geta verið mjög breytileg eftir því hve svæsin röskunin er og einnig hve hratt hún gerist. Þó er oft samsvörun við serum gildi en fyrstu einkenni eru slappleiki, sljóleiki, höfuðverkur, ógleði og uppköst. Þegar gildi fer að nálgast 110mmol/l er að bera á rugli, flogum og meðvitundarleysi, sérstaklega ef lækkun er hröð (<48 klst). Hyponatraemia getur verið vegna þynningar (hypervolaemia) eða taps á salti umfram vökva (hypovolaemia). Í upphafi er því mikilvægt að átta sig á hvert vökvajafnvægi sjúklingsins er klínískt og mæla einnig serum og þvag natrium og osmolality áður en nokkuð inngrip hefur farið fram. Flestir sem hafa spot þvag Na+ < 30mmol/l eru hypovolaemiskir og munu svara saltvatnsinfusion en flestir aðrir hafa óviðeigandi losun á AVP eða Syndrome of Inappropriate ADH (SIADH).
Ein algengasta orsök hyponatraemiu er lyfjameðferð með þíasíð þvagræsilyfjum. Orsökin þarna er minnkað effective plasma volume og ADH er hærra en við má búast en auk þess saltsóun (ekki að marka þvag Na+ gildi). Í hypothyroidisma er AVP losun hærri en búast má við, etv. vegna örvunar baroreceptora í atrium vegna minnkaðs cardiac output í þessu ástandi. Þetta er þó óljóst. Skortur á kortisóli getur einnig valdið óeðlilega háu AVP og hyponatraemiu, líklega vegna röskuna á neikvæðri afturvirkni þegar kortisol vantar (AVP via V1b stýrir ACTH losun) en kortisól hefur reyndar einnig bein áhrif á nýru.
Aðrar orsakir SIADH eru lyf svo sem krabbameinslyf, geðlyf ofl. en einnig efni eins og ecstacy. Lungnabólga, lungnakrabbamein, höfuðáverkar ofl eru einnig þekktar orsakir SIADH.
Á undanförnum árum hafa komið fram tilfelli hyponatraemiu hjá langhlaupurum en líklega gerist þetta hjá um 15% hlaupara. Þetta er talið fyrst og fremst vera vegna of mikillar neyslu vökva í hlaupum en misskilinn áróður er rekinn fyrir þessu. Sömuleiðis virðist AVP ekki bælast fullkomlega hjá þessum einstaklingum og því má segja að þeir hafi form af SIADH. Sumir hlauparar nota einnig NSAI lyf sem auka næmi nýrna fyrir AVP. Lykillinn er að taka ekki NSAID fyrir hlaup og takmarka neyslu vökva þannig að einungis sé drukkið við þorsta.
Á undanförnum árum hefur einnig byggst upp þekkingargrunnur um tengsl langvinnrar hyponatraemiu við beinþynnnigu.
Stöku sinnum finnst ekki orsök hyponatraemiunnar og þá um raunverulegt krónískt SIADH að ræða. Hér mætti gefa lyf sem draga úr virkni AVP á nýru eins og liþíum eða demeclocylcline en einnig eru í þróun lyf sem væntanleg eru á markað sem eru V2 viðtaka blokkar. Þessi lyfjaflokkur kallast vaptans, t.d. conivaptan og tolvaptan.
Klínísk uppvinnsla hyponatraemiu hefst þannig á því að meta klínískt vökvajafnvægi sjúklings, mæla osmolality og natrium í sermi og þvagi og skoða lyfjasögu - allt áður en settur er upp vökvi (sem er erfitt á BMT). Hafa þarf svo í huga hypothyroidisma og skort á kortisóli.
Ein algengasta orsök hyponatraemiu er lyfjameðferð með þíasíð þvagræsilyfjum. Orsökin þarna er minnkað effective plasma volume og ADH er hærra en við má búast en auk þess saltsóun (ekki að marka þvag Na+ gildi). Í hypothyroidisma er AVP losun hærri en búast má við, etv. vegna örvunar baroreceptora í atrium vegna minnkaðs cardiac output í þessu ástandi. Þetta er þó óljóst. Skortur á kortisóli getur einnig valdið óeðlilega háu AVP og hyponatraemiu, líklega vegna röskuna á neikvæðri afturvirkni þegar kortisol vantar (AVP via V1b stýrir ACTH losun) en kortisól hefur reyndar einnig bein áhrif á nýru.
Aðrar orsakir SIADH eru lyf svo sem krabbameinslyf, geðlyf ofl. en einnig efni eins og ecstacy. Lungnabólga, lungnakrabbamein, höfuðáverkar ofl eru einnig þekktar orsakir SIADH.
Á undanförnum árum hafa komið fram tilfelli hyponatraemiu hjá langhlaupurum en líklega gerist þetta hjá um 15% hlaupara. Þetta er talið fyrst og fremst vera vegna of mikillar neyslu vökva í hlaupum en misskilinn áróður er rekinn fyrir þessu. Sömuleiðis virðist AVP ekki bælast fullkomlega hjá þessum einstaklingum og því má segja að þeir hafi form af SIADH. Sumir hlauparar nota einnig NSAI lyf sem auka næmi nýrna fyrir AVP. Lykillinn er að taka ekki NSAID fyrir hlaup og takmarka neyslu vökva þannig að einungis sé drukkið við þorsta.
Á undanförnum árum hefur einnig byggst upp þekkingargrunnur um tengsl langvinnrar hyponatraemiu við beinþynnnigu.
Stöku sinnum finnst ekki orsök hyponatraemiunnar og þá um raunverulegt krónískt SIADH að ræða. Hér mætti gefa lyf sem draga úr virkni AVP á nýru eins og liþíum eða demeclocylcline en einnig eru í þróun lyf sem væntanleg eru á markað sem eru V2 viðtaka blokkar. Þessi lyfjaflokkur kallast vaptans, t.d. conivaptan og tolvaptan.
Klínísk uppvinnsla hyponatraemiu hefst þannig á því að meta klínískt vökvajafnvægi sjúklings, mæla osmolality og natrium í sermi og þvagi og skoða lyfjasögu - allt áður en settur er upp vökvi (sem er erfitt á BMT). Hafa þarf svo í huga hypothyroidisma og skort á kortisóli.
Marklýsing
- Vita um helstu lífeðlisfræðilegu ferla sem undirstúka tekur þátt í.
- Þekkja stýriferla undirstúku, heiladinguls og markvefja.
- Þekkja tegundir og virkni umræddra hormóna ásamt stýrikerfum þeirra.
- Gróf faraldsfræði og innbyrðis algengi æxla í heiladingli.
- Þekkja klíníska mynd of eða vanseytingar hormóna og einkenni heiladingulsæxla. Geta gert sér grein fyrir klínískri nálgun.
- Fyrstu rannsóknir og meðferð í grófum dráttum við sjúkdómum í undirstúku og heiladingli
- Geta rætt þá ferla og þætti sem stýra jafnvægi vatns í líkama
- Geta lagt upp áætlun um rannsóknir og viðbrögð við hyponatraemiu
- Geta reiknað út osmolality